«Регуляторные исследования и экспертиза лекарственных средств» – научно-практический рецензируемый журнал открытого доступа, выпускаемый в печатной и онлайн-версиях. Основан в 1999 году.
Цель журнала: содействие развитию фармацевтической и медицинской науки и практики посредством опубликования и распространения информации о передовых достижениях в регуляторной деятельности и сфере обращения лекарственных средств.
Целевая аудитория. Предназначен для широкого круга специалистов, как российских, так и зарубежных, работающих в сфере обращения лекарственных средств:
- разработчиков и производителей лекарственных препаратов;
- представителей экспертных организаций, государственных регуляторных органов;
- работников контрольно-разрешительной системы и государственного надзора в сфере обращения лекарственных средств;
- сотрудников научно-исследовательских институтов, преподавателей, аспирантов и студентов медицинских, фармацевтических вузов, врачей и провизоров.
Более подробная информация – в разделе Цели и задачи.
Учредитель: ФГБУ «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации.
Периодичность: 6 раз в год.
Импакт-фактор: двухлетний импакт-фактор РИНЦ (2024) – 0,533.
Редколлегия. Географическое представительство:
- 8 стран
- 12 городов
Рецензирование:
- Двойное слепое
- Минимум 2 рецензента на рукопись
Основные метрики журнала:
14 дней в среднем от подачи до первого решения
88 дней в среднем от подачи до публикации в Интернете
15% приглашенных авторов
68% доля принятия рукописей
64 тыс. загрузок PDF в 2025 г.
Плата за публикацию: бесплатно.
Индексация. Индексируется в российских и международных реферативных и полнотекстовых базах, включен в наукометрические базы данных РИНЦ, RSCI, входит в "Белый список" научных изданий и Перечень ВАК (категория К1).
Информация об индексации в других российских и международных базах доступна в разделе Индексирование.
Регистрация. Свидетельство о регистрации средства массовой информации ПИ № ФС77-82931 от 14 марта 2022 г.
Подписка. Подписной индекс в каталоге Пресса России – 57942, Урал-Пресс – 57942.
Текущий выпуск
ГЛАВНАЯ ТЕМА: ФАРМАКОТЕРАПИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ: РАЗРАБОТКА И КОНТРОЛЬ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ
Хроническая сердечная недостаточность (ХСН) остается одной из ключевых медико-социальных проблем, определяющих прогноз и качество жизни пациентов. Современная фармакотерапия смещает акцент с симптоматического лечения на раннее вмешательство и модификацию прогноза, что требует строгой доказательной и регуляторной оценки и использования инновационных лекарственных препаратов. В этом контексте особый интерес представляет экспертный взгляд на эволюцию фармакотерапии ХСН, поиск новых терапевтических мишеней и перспективы трансляции фундаментальных исследований в клиническую практику через призму науки, клинического опыта и регуляторной логики. Этим и другим вопросам посвящено интервью с директором Клиники госпитальной терапии имени А.А. Остроумова и Центра сердечной недостаточности Сеченовского Университета, президентом российского Общества специалистов по сердечной недостаточности академиком РАН Ю.Н. Беленковым.
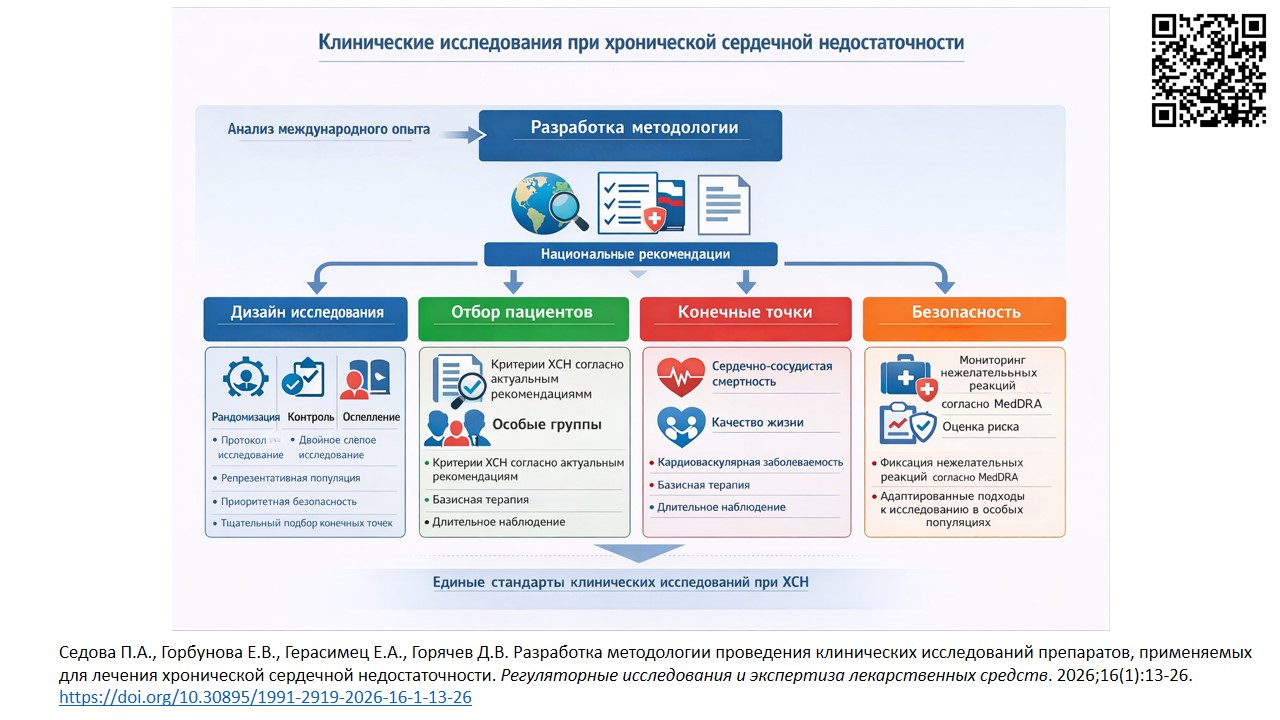
ВВЕДЕНИЕ. Проблема хронической сердечной недостаточности (ХСН) в настоящее время приобретает все большую актуальность не только для клинической медицины, но и для всей системы здравоохранения и общества в целом. Высока необходимость разработки новых лекарственных препаратов, в том числе комбинированных, для лечения ХСН. На данный момент в России и странах Евразийского экономического союза отсутствуют нормативные и методические документы или руководства, регламентирующие вопросы планирования, проведения и оценки клинических исследований лекарственных средств для терапии пациентов с ХСН, в связи с чем поставлена задача разработки подобного руководства с учетом национальных требований к регистрации лекарственных препаратов.
ЦЕЛЬ. Систематизация международных подходов к клиническим исследованиям препаратов, применяемых для лечения хронической сердечной недостаточности, для последующей разработки соответствующего руководства, действующего на территории Российской Федерации.
ОБСУЖДЕНИЕ. Основными принципами проведения клинических исследований препаратов для лечения ХСН являются: рандомизация, контроль, ослепление, клинически значимые конечные точки, репрезентативность популяции и приоритизация безопасности. Стандартом оценки эффективности и безопасности лекарственного препарата следует считать рандомизированное контролируемое исследование с применением метода двойного ослепления. Подтверждение эффективности терапии также требует тщательного отбора пациентов по четким критериям диагностики ХСН, достаточного объема выборки и длительности наблюдения, идентичности сопутствующей базисной терапии, разработки адаптированных подходов к исследованию в особых популяциях пациентов (педиатрическая и геронтологическая популяции). Выбор конечных точек зависит от их влияния на прогноз заболевания и качество жизни пациентов, а также значения препарата в терапии. Следует отметить, что в настоящее время больше внимания уделяется пациент-ориентированным исходам (улучшению самочувствия) при условии обеспечения безопасности и отсутствия негативного влияния на выживаемость.
ВЫВОДЫ. Принципы проведения клинических исследований при хронической сердечной недостаточности как в национальной российской среде, так и за рубежом едины и опираются на фундаментальные постулаты доказательной медицины. Внедрение описанных научно обоснованных принципов клинических исследований препаратов для терапии ХСН будет способствовать повышению стандартов лечения, что, в конечном итоге, должно положительно отразиться на прогнозах и исходах заболевания.
ВВЕДЕНИЕ. Согласно утвержденной российской нормативной документации для определения подлинности лекарственных средств, содержащих сердечные гликозиды ландыша (Convallaria majalis), используют общегрупповые качественные реакции и метод тонкослойной хроматографии; для количественной оценки гликозидов применяют метод спектрофотометрии и биологический метод определения. Постепенный отказ от испытаний на животных, а также тот факт, что методики, основанные на биологическом методе, не характеризуются высокой точностью и воспроизводимостью, обусловливают необходимость разработки новых, физико-химических методов контроля качества лекарственных препаратов ландыша.
ЦЕЛЬ. Замена in vivo методики количественного определения сердечных гликозидов в лекарственных препаратах ландыша на методику, основанную на физико-химическом методе анализа.
МАТЕРИАЛЫ И МЕТОДЫ. Объектами исследования являлись лекарственные средства отечественного производства: «Ландыша настойка» и «Зеленина капли»; стандартный образец экстракта ландыша, стандартный образец конваллятоксина (93,0%). Оценка биологической активности выполнена согласно фармакопейной методике на озерных лягушках (Rana ridibunda). Содержание конваллятоксина определено методом высокоэффективной жидкостной хроматографии (ВЭЖХ) по методике, разработанной авторами. Проведена оценка ранговой корреляции с использованием коэффициента Спирмена между данными, полученными биологичеcким методом и методом ВЭЖХ, а также ВЭЖХ и спектрофотометрией.
РЕЗУЛЬТАТЫ. Показана возможность использования методики ВЭЖХ для качественной и количественной оценки препаратов, содержащих сердечные гликозиды ландыша. Определено среднее содержание доминирующего и наиболее биологически активного гликозида — конваллятоксина методом ВЭЖХ в препаратах ландыша: стандартный образец экстракта ландыша 0,14578 мг/мл; ландыша настойка 0,01397 мг/мл; Зеленина капли 0,00630 мг/мл; также определена биологическая активность объектов исследования. С помощью коэффициента ранговой корреляции Спирмена проведен корреляционный анализ результатов исследования.
ВЫВОДЫ. Для идентификации и количественного определения в лекарственных средствах «Ландыша настойка» и «Зеленина капли» конваллятоксина предложена методика, основанная на методе ВЭЖХ, позволяющая получать воспроизводимые и точные результаты. Рекомендуемые нормы содержания конваллятоксина: «Ландыша настойка» 0,01–0,02 мг/мл; «Зеленина капли» 0,004–0,008 мг/мл.
ВВЕДЕНИЕ. Одной из основных групп лекарственных препаратов для терапии сердечно-сосудистых заболеваний являются β-блокаторы, в частности бисопролола фумарат, характеризующийся высокой селективностью к β-рецепторам первого типа. В Государственную фармакопею Российской Федерации XV изд. (ГФ РФ) включена фармакопейная статья (ФС) на фармацевтическую субстанцию бисопролола фумарата, однако ФС на лекарственный препарат отсутствует. Зарубежные фармакопеи устанавливают разные требования к контролю качества лекарственных средств бисопролола фумарата. В связи с этим представляется целесообразным систематизировать информацию по национальным и зарубежным фармакопейным требованиям к лекарственным препаратам и фармацевтическим субстанциям бисопролола фумарата.
ЦЕЛЬ. Систематизация требований к качеству лекарственных средств для подготовки рекомендаций по составлению спецификаций на препарат бисопролола фумарата в лекарственной форме «таблетки» и фармацевтическую субстанцию бисопролола фумарата.
МАТЕРИАЛЫ И МЕТОДЫ. В работе использовали методы сравнительного информационно-аналитического исследования и контент-анализа. Проведено исследование требований ГФ РФ XV изд. и монографий следующих фармакопей: Европейской (Ph. Eur.), Британской (ВР), США (USP), Китайской Народной Республики (ChP), Японской (JP), Республики Корея (KP) и Индийской (IP) к качеству лекарственных средств бисопролола фумарата и материалов регистрационных досье.
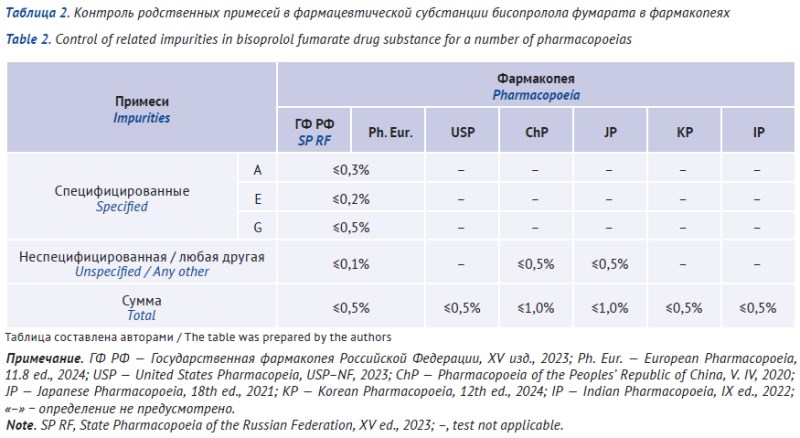
РЕЗУЛЬТАТЫ. ГФ РФ и зарубежные фармакопеи Ph. Eur., USP, IP, ChP, JP и KP содержат ФС и монографии на фармацевтическую субстанцию бисопролола фумарата. На препарат бисопролола в лекарственной форме «таблетки» отсутствуют национальные стандарты качества, монографии на данную лекарственную форму включены в BP, USP, ChP и JP. Проведен сравнительный анализ ФС ГФ РФ и монографий зарубежных фармакопей. ФС «Бисопролола фумарат» ГФ РФ XV изд. в целом гармонизирована с требованиями Ph. Eur., однако имеются различия в части подтверждения подлинности действующего вещества и необходимости контроля фумаровой кислоты. Изучены материалы регистрационных досье на фармацевтические субстанции и препараты бисопролола фумарата. Обоснована необходимость «гибкого подхода» к контролю органических примесей в фармацевтических субстанциях и лекарственных препаратах, проведению испытания на растворение, возможность использования альтернативных комбинаций методов высокоэффективной жидкостной хроматографии (ВЭЖХ) и тонкослойной хроматографии либо ВЭЖХ и спектрофотометрии для препарата.
ВЫВОДЫ. В результате проведенного исследования обоснован выбор показателей качества и методов анализа для идентификации, испытания на растворение для подготовки рекомендаций по составлению спецификаций на препараты бисопролола фумарата в лекарственной форме «таблетки». Установлены примеси, относящиеся к технологическим примесям синтеза фармацевтической субстанции и продуктам деградации, что также может быть использовано для подготовки рекомендаций по составлению спецификаций. Обоснована необходимость оценки и контроля возможности образования генотоксичных примесей при получении фармацевтических субстанций.
ВВЕДЕНИЕ. Карведилол — препарат, применяемый при лечении реноваскулярной артериальной гипертензии и заболеваний сердечно-сосудистой системы. Фармакопейная статья на фармацевтическую субстанцию карведилола включена в Государственную фармакопею Российской Федерации (ГФ РФ), однако требования к качеству лекарственных препаратов на основе карведилола в ГФ РФ отсутствуют. Для разработки фармакопейной статьи на лекарственные препараты карведилола необходима систематизация действующих зарубежных и российских требований к лекарственным средствам на основе карведилола.
ЦЕЛЬ. Разработка подхода к контролю качества лекарственного препарата в лекарственной форме «таблетки» и фармацевтической субстанции карведилола.
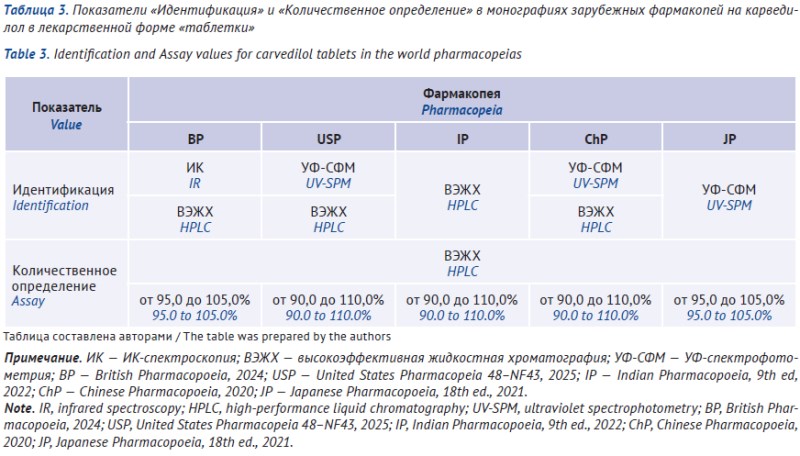
ОБСУЖДЕНИЕ. По данным Государственного реестра лекарственных средств, в обращении на территории Российской Федерации находятся фармацевтические субстанции карведилола 7 производителей и зарегистрировано 18 препаратов карведилола в лекарственной форме «таблетки» (из них в ЕАЭС зарегистрировано 11). Фармацевтическая субстанция карведилола описана в ГФ РФ XV изд. и в ведущих зарубежных фармакопеях: Европейской фармакопее (Ph. Eur.), Британской фармакопее (ВР), Американской фармакопее (USP), Индийской фармакопее (IP), Фармакопее Китайской Народной Республики (ChP), Японской фармакопее (JP), Корейской фармакопее (КР). Монография на лекарственную форму «таблетки карведилола» включена в ряд ведущих зарубежных фармакопей — ВР, USP, IP, ChP, JP, в ChP также включена монография на лекарственную форму «капсулы». Проведен сравнительный анализ требований по ключевым показателям качества: «Идентификация», «Родственные примеси», «Количественное определение» для субстанции и для таблеток; дополнительно для таблеток — «Растворение». Показано, что подходы к нормированию примесей и испытанию «Растворение» существенно различаются между фармакопеями; базовыми для контроля примесей являются методики на основе высокоэффективной жидкостной хроматографии (ВЭЖХ), базовым методом идентификации — ИК-спектроскопия.
ВЫВОДЫ. На основе сравнительного анализа фармакопейных документов предложен унифицированный подход к формированию требований к качеству лекарственных средств карведилола (субстанции и таблетки): выбор приоритетных показателей качества, обоснование аналитических методов (ИК-спектроскопия, ВЭЖХ, титриметрия/ВЭЖХ для количественного определения, растворение) и установление нормативных требований с учетом риск-ориентированного контроля примесей. Предложенный подход может быть использован при экспертизе материалов регистрационного досье и подготовке проекта фармакопейной статьи на таблетки карведилола для ГФ РФ.
РАЗРАБОТКА ЛЕКАРСТВЕННЫХ СРЕДСТВ
ВВЕДЕНИЕ. Пероральное применение пробиотиков затруднено ввиду их низкой выживаемости в агрессивной среде желудочно-кишечного тракта. Микрокапсулирование в альгинат-хитозановой системе позволяет защитить бактериальные клетки и обеспечить их доставку в толстый кишечник. В настоящее время недостаточно изучено влияние условий покрытия альгинатных микрокапсул хитозаном и соотношение профилей высвобождения модельных субстанций к выживаемости микрокапсулированных пробиотиков; решение требует экспериментального сопоставления параметров покрытия, размера микрокапсул и их влияния на высвобождение и КОЕ.
ЦЕЛЬ. Сформировать методические рекомендации для разработки лекарственных форм пробиотических культур на примере Bifidobacterium bifidum.
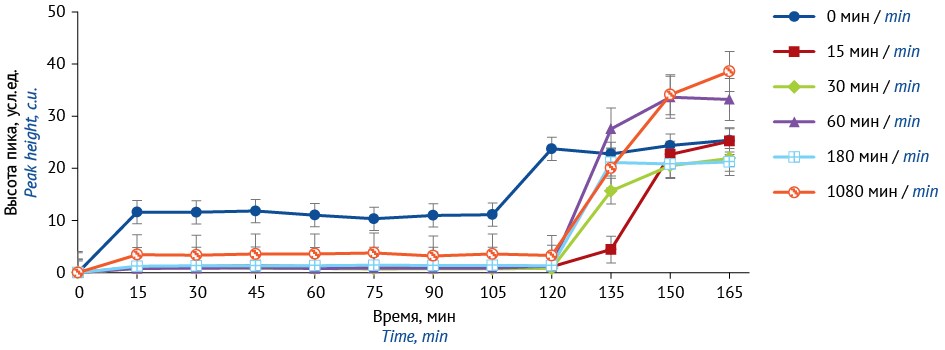
МАТЕРИАЛЫ И МЕТОДЫ. Использованы 2% раствор альгината натрия с метамизолом натрия (2%) или бифидобактериями (2,5×10⁶/1,25×10⁶ КОЕ/мл), который экструдировали в 5% CaCl2 с последующим покрытием микрокапсул хитозаном (0,4%, pH 6,0) путем выдержки в растворе хитозана 0–1080 мин; экструзия через иглы 0,16 и 1,8 мм; тест растворения с изменением pH без замены среды; количественное определение метамизола натрия методом УФ-спектрофотометрии (λ = 258 нм); выживаемость — подсчет количества КОЕ методом посева на питательной среде МРС-5.
РЕЗУЛЬТАТЫ. Покрытие микрокапсул хитозаном уже при 15 мин выдержки в растворе существенно снижало раннее высвобождение метамизола натрия, при последующем увеличении времени выдержки микрокапсул в растворе хитозана изменения были несущественны. Выживаемость бифидобактерий: игла 0,16 мм без покрытия <1%; игла 0,16 мм с покрытием ~20% (при введении в обоих случаях бифидобактерий в микрокапсулы в количестве 0,5×10⁹ КОЕ); игла 1,8 мм с покрытием ~50% при введении бифидобактерий в микрокапсулы в количестве 0,5×10⁹ КОЕ и ~80% при введении бифидобактерий в микрокапсулы в количестве 1×10⁹ КОЕ.
ВЫВОДЫ. Кратковременная выдержка микрокапсул в хитозане формирует функциональный барьер, уменьшающий преждевременное высвобождение содержимого и повышающий выживаемость микрокапсулированных пробиотиков; увеличение размера микрокапсул значительно повышает их защитные свойства. Для промышленной технологии микрокапсулирования пробиотиков рекомендуется покрытие хитозаном с выдержкой ~15 мин (0,4% хитозана, pH 6,0) как базовые условия. Для достижения максимальной выживаемости и удобства дозирования предпочтительно использование больших игл для экструзии с последующей упаковкой, защищающей от влаги и кислорода (Alu/Alu блистеры или флаконы с влагопоглотителем).
ВВЕДЕНИЕ. Несмотря на обширный арсенал гипогликемических средств, выбор их лекарственных форм, особенно пролонгированного действия, остается ограниченным. В связи с этим необходима разработка инъекционных депо-форм, обеспечивающих длительное и контролируемое высвобождение действующего вещества. Ключевым этапом и одним из определяющих факторов для создания стабильной парентеральной депо-формы является изучение растворимости действующего вещества и подбор растворителя или их смеси, обеспечивающих эффективное высвобождение соединения во внешнюю среду. Гликлазид, один из самых часто назначаемых гипогликемических препаратов, доступен лишь в формах для перорального приема, ввиду чего задача создания его пролонгированной формы для парентерального введения является актуальной, решение этой задачи позволит оптимизировать терапию для широкого круга пациентов.
ЦЕЛЬ. Разработка пролонгированной депо-системы гликлазида для парентерального введения.
МАТЕРИАЛЫ И МЕТОДЫ. Определение растворимости гликлазида в биосовместимых растворителях проводили по фармакопейной методике: в стандартных условиях и при нагревании. Биофармацевтические исследования in vitro проводили методом диализа через целлофановую мембрану. Количественное определение гликлазида в пробах диализата проводили методом УФ-спектрофотометрии (λ=230 нм). Антидиабетическую активность исследуемых объектов проводили на модели сахарного диабета, индуцированного аллоксаном, у самцов крыс линии Wistar возрастом 7–8 нед. Уровень глюкозы в крови животных контролировали с помощью глюкометра Accu-Chek® Performa Nano в течение 24 ч после однократного введения исследуемых образцов.
РЕЗУЛЬТАТЫ. Результаты оценки растворимости гликлазида свидетельствуют о лучшей растворимости гликлазида в диметилсульфоксиде и спирте этиловом 95%. Гликлазид практически нерастворим в полиэтиленгликоле-400, пропиленгликоле-1,2, изопропилмиристате, глицерине и мало растворим в спирте этиловом 70%. При повышении температуры растворимость гликлазида в пропиленгликоле-1,2 и полиэтиленгликоле-400 увеличивается до значений «малорастворим». Высвобождение гликлазида из водной модели суспензии в течение 2 ч составило 15,69±0,49%. Определен сопоставимый антидиабетический эффект для инъекционных моделей депо-форм, приготовленных с использованием бинарных дисперсионных сред: воды для инъекций, пропиленгликоля-1,2 и диметилсульфоксида. Более выраженный гипогликемический эффект наблюдали при использовании в качестве дисперсионной среды смеси воды для инъекций и пропиленгликоля-1,2, а также смеси диметилсульфоксида и пропиленгликоля-1,2.
ВЫВОДЫ. Получены модельные составы инъекционных депо-форм гликлазида пролонгированного действия на основе бинарных систем, проведена их биофармацевтическая оценка. В результате исследования показана необходимость введения в состав суспензии органических растворителей, способных повысить высвобождение гликлазида из водной суспензии.
ДОКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
ВВЕДЕНИЕ. В настоящее время доклиническая разработка анальгетических препаратов в значительной степени ограничена валидностью моделей и методов оценки боли. Для преодоления трансляционного барьера при разработке обезболивающих средств необходимы ревизия существующих методов оценки болевой чувствительности и разработка новых подходов, которые включают исследование не только рефлекторного, но и аффективного компонента боли.
ЦЕЛЬ. Систематизация современных представлений о методах оценки боли у лабораторных животных и определение критериев их применимости в доклинических исследованиях новых анальгетиков.
ОБСУЖДЕНИЕ. Обзор основан на анализе 75 научных публикаций (оригинальные исследования и систематические обзоры за последние 35 лет). Боль — многомерный феномен, включающий сенсорно-дискриминационный и аффективно-мотивационный компоненты. Стандартные ноцицептивные тесты характеризуются высокой оценочной эффективностью в отношении сенсорной гиперчувствительности, но оказываются недостаточно чувствительными для изучения хронической боли, в основе которой лежит аффективный компонент. Менее широко используемые нерефлекторные методы (шкала гримас, ультразвуковая вокализация, тест рытья нор) хотя и позволяют оценивать аффективный компонент, часто обладают низкой специфичностью и недостаточно валидированы на различных моделях боли. Комбинированный, полимодальный подход повышает объективность, воспроизводимость и трансляционную предиктивность доклинических исследований на пути к разработке новых анальгетиков.
ВЫВОДЫ. Ноцицептивные тесты являются инструментом оценки эффективности обезболивающих средств как в рамках первичного скрининга, так и на этапе доклинических исследований. Стандартные ноцицептивные тесты не позволяют оценить аффективный компонент боли, поэтому разработка новых обезболивающих препаратов требует включения в программу доклинических исследований нерефлекторных методов оценки боли. Совместное использование рефлекторных и нерефлекторных методов оценки боли является основой разработки новых исследовательских стратегий в доклинических исследованиях.
КОНТРОЛЬ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ
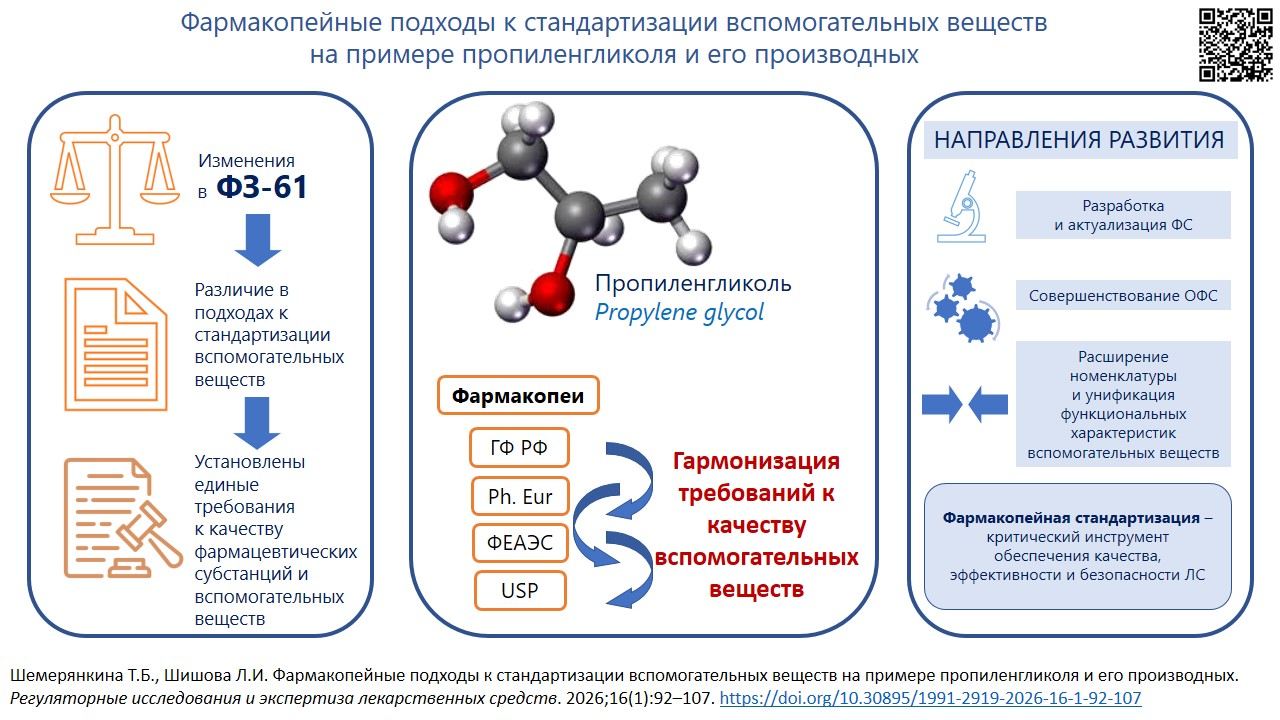
ВВЕДЕНИЕ. Внесение изменений в Федеральный закон № 61-ФЗ «Об обращении лекарственных средств», в соответствии с которым общие фармакопейные статьи (ОФС) и фармакопейные статьи (ФС) должны быть дополнены указаниями о вспомогательных веществах (ВВ), обусловливает необходимость на законодательном уровне совершенствовать требования к стандартизации ВВ.
ЦЕЛЬ. Определение основных направлений развития фармакопейных подходов к стандартизации вспомогательных веществ на примере пропиленгликоля и его производных.
ОБСУЖДЕНИЕ. Рассмотрено понятие «вспомогательное вещество» и требования к стандартизации ВВ на национальном, региональном и международном уровнях. Установлено, что понятие «субстанция для фармацевтического применения» наиболее корректно определяет фармакопейные подходы к стандартизации ВВ. Выявлено, что вопрос о количестве наименований ВВ, входящих в состав лекарственных препаратов, обращающихся на фармацевтическом рынке Российской Федерации, остается актуальным. Проведен сравнительный анализ подходов Государственной фармакопеи Российской Федерации, Фармакопеи ЕАЭС и зарубежных фармакопей (Фармакопеи США, Европейской фармакопеи, Фармакопеи КНР) к стандартизации общих требований к качеству ВВ и конкретных требований к стандартизации пропиленгликоля и его производных. Установлено, что фармакопейные требования к качеству ВВ основаны на комплексном подходе, включающем определение общих показателей качества для субстанций и оценку дополнительных показателей качества, зависящих от функциональных характеристик (ФХ). Сопоставлен перечень наименований ФХ, приведенный в фармакопейных требованиях различных государств, отмечено, что обозначение ФХ не всегда унифицировано.
ВЫВОДЫ. Фармакопейный подход к стандартизации ВВ является критически важным инструментом в контроле и обеспечении качества, эффективности и безопасности лекарственных препаратов. Обозначены основные фармакопейные подходы к стандартизации ВВ с учетом анализа данных о контроле качества ПГ и его производных: продолжение дальнейшей разработки и актуализации ФС на ВВ; совершенствование требований к универсальным показателям качества ВВ в соответствии с ОФС «Субстанции для фармацевтического применения» и установлению требований к ФХ; расширение номенклатуры ВВ, включаемых в Государственную фармакопею Российской Федерации, увеличение количества фармакопейных стандартов на конкретные ВВ на основе анализа и гармонизации национальных, региональных и международных требований.
ВВЕДЕНИЕ. Отсутствие национальных требований, регламентирующих качество фармацевтической субстанции валацикловира гидрохлорида в гидратной форме и лекарственных препаратов валацикловира, может вызывать затруднения у производителей лекарственных препаратов, а также у экспертов при проведении экспертизы материалов регистрационного досье. Для разработки нормативных документов, устанавливающих требования к качеству, необходимо выполнить анализ имеющихся фармакопейных требований к другим лекарственным средствам на основе валацикловира. В связи с этим представляется актуальным анализ фармакопейных требований к качеству фармацевтической субстанции валацикловира гидрохлорида и лекарственных препаратов валацикловира для заявителей при подготовке регистрационного досье и экспертов при проведении экспертизы качества лекарственных средств.
ЦЕЛЬ. Анализ и обобщение требований к качеству лекарственных средств на основе валацикловира: фармацевтических субстанций в безводной и гидратной формах и препаратов в лекарственной форме «таблетки».
МАТЕРИАЛЫ И МЕТОДЫ. Проведено сравнительное изучение требований к качеству фармацевтических субстанций валацикловира гидрохлорида, описанных в Государственной фармакопее Российской Федерации XV изд., в других фармакопеях (Европейской (Ph. Eur.), Британской (ВР), Фармакопее США (USP), Индийской (IP), Китайской (ChP), Японской (JP)), материалах регистрационных досье лекарственных препаратов валацикловира гидрохлорида в лекарственной форме «таблетки», описанных в монографиях BP, USP, IP, ChP, JP.
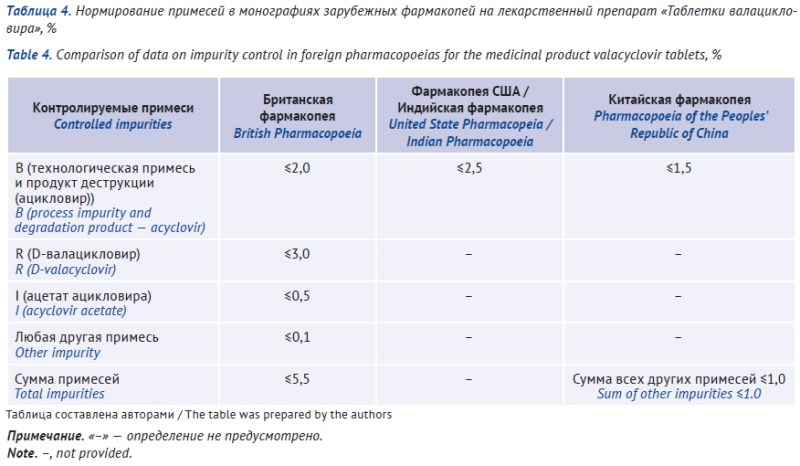
РЕЗУЛЬТАТЫ. Валацикловира гидрохлорид — лекарственное средство, применяющееся при лечении герпесвирусных инфекций. В Государственный реестр лекарственных средств включены фармацевтические субстанции 6 производителей, 17 препаратов в лекарственной форме «таблетки, покрытые пленочной оболочкой» (из них в ЕАЭС зарегистрировано 14). Фармакопейные статьи (монографии) на фармацевтическую субстанцию валацикловира гидрохлорида включена в Государственную фармакопею Российской Федерации XV изд., Ph. Eur., BP, USP, IP, ChP, JP. Ph. Eur., BP, USP и IP устанавливают требования на безводную и гидратную формы валацикловира. В Ph. Eur. и BP профиль примесей безводной и гидратной форм валацикловира существенно различается, в других фармакопеях отличия только в содержании воды. Препарат валацикловира в лекарственной форме «таблетки» описан в BP, USP, IP, ChP и JP. Для идентификации валацикловира следует применять либо метод ИК-спектрометрии, либо 2 метода: ВЭЖХ и УФ-спектрофотометрию; предусмотреть нормирование идентифицированной примеси ацикловира, неспецифицируемых примесей и суммы примесей (органические примеси). Несмотря на разный профиль примесей для фармацевтической субстанции в гидратной и безводной формах, для таблеток в BP требования идентичны независимо от используемой субстанции.
ВЫВОДЫ. Проведенный анализ зарубежных фармакопей и материалов регистрационных досье позволяет обобщить требования к контролю примесей в фармацевтической субстанции валацикловира и в препаратах в лекарственной форме «таблетки» при различающихся способах синтеза фармацевтической субстанции. Определены альтернативные варианты методов для идентификации действующего вещества в лекарственных препаратах валацикловира. По результатам сравнительного анализа показаны различия норм в испытании на растворение в фармакопеях, что может быть реализовано в спецификациях производителей, поскольку данный тест подтверждает устойчивость технологического процесса, однородность серий, качество лекарственного препарата, а не его сопоставимость с аналогами.
Объявления
2025-06-03
Поздравляем с избранием в академики РАН!
Редколлегия и редакция журнала «Регуляторные исследования и экспертиза лекарственных» поздравляют члена редколлегии – Андрея Дмитриевича Дурнева, избранного в действительные члены Российской академии наук.
| Еще объявления... |
ISSN 3034-3453 (Online)